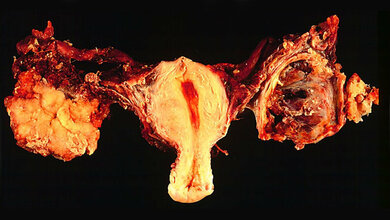
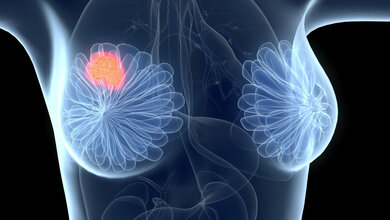
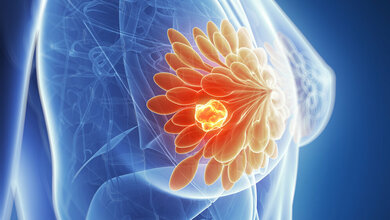
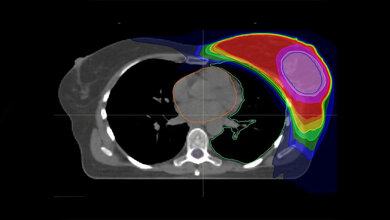
Ein zentraler Marker für Brust- und Eierstockkrebs ist BRCA1 (engl. BReast CAncer Gene 1), ein Protein, das im körpereigenen Reparaturmechanismus der DNA eine wichtige Rolle spielt. Eine Mutation des BRCA1-Gens erhöht das Risiko des Auftretens von malignen Tumoren. Laut Zentrum für Familiären Brust- und Eierstockkrebs des AKH Wiens geht man davon aus, dass bei verändertem BRCA1 oder BRCA2 Gen bei Frauen die Wahrscheinlichkeit an Brustkrebs zu erkranken bei bis zu 85%, und die Wahrscheinlichkeit an Eierstockkrebs zu erkranken bei bis zu 53% liegt. Während Mutationen in BRCA1/BRCA2 unkontrolliertes Zellwachstum unterstützen, führen sie auch zur Destabilisierung des genetischen Materials der Krebszelle. Dadurch sind solche Krebszellen auf andere Reparaturmechanismen angewiesen, die diese Destabilisierung kompensieren. Entsprechend bezeichnen Wissenschaftler/-innen die Abhängigkeit der Zellen mit mutiertem BRCA1 oder BRCA2 Gen von anderen Genen auch als „Achilles-Ferse“ von Krebszellen, da das Zurückgreifen auf andere DNA-Reparaturgene zu einer synthetisch letalen Beziehung, zu Abhängigkeiten, führen kann.
Vorteile gegenüber traditioneller Chemotherapie
Joanna Loizou, vormals Forschungsgruppenleiterin am CeMM sowie Associate Professor am Comprehensive Cancer Center der Medizinischen Universität Wien, erklärt: „Die Synthetische Letalität als Therapiekonzept zur Behandlung von Brust- und Eierstockkrebs erlaubt es, spezifisch die Teilung von Krebszellen zu unterbinden, während gesunde Zellen davon nicht betroffen sind. Wir hemmen dabei jene Gene, von denen ein mutiertes BRCA1 abhängig ist. Derartige Therapiekonzepte haben im Allgemeinen viele Vorteile gegenüber traditioneller Chemotherapie.“
POLΘ untersucht
Studienautorin Anna Schrempf widmete sich gemeinsam mit Co-Autorin Sara Bernardo dem Gen POLΘ (DNA-Polymerase theta), das ebenso Teil des zellulären DNA-Reparaturmechanismus und mit BRCA1 synthetisch letal ist. POLΘ ist eine DNA-Polymerase, die eine Schlüsselrolle bei der Reparatur von DNA-Doppelstrangbrüchen spielt. In ihrer Studie konnten die Wissenschaftler/-innen zeigen, dass POLΘ darüber hinaus auch beim Einzelstrangbruch der DNA, der besonders bei BRCA1 mutierten Zellen auftritt, aktiviert wird und die dabei entstehenden Lücken füllt. „Im Gegensatz zu früheren Studien zeigen wir damit eine bisher unbeschriebene Funktion von POLΘ. Ein besseres Verständnis von POLΘ gibt grundlegenden Aufschluss über die DNA-Reparaturmechanismen und zeigt, dass POLΘ eine wichtige Rolle in der DNA-Replikation spielt. Durch das medikamentöse Inhibieren von POLΘ können wir das genetische Material von Krebszellen mit mutiertem BRCA1 destabilisieren, weitere Zellteilungen verlangsamen und so das Wachstum stoppen“, erklärt Schrempf.
Zusätzliche, potenzielle Therapiepfade im Blick
Ein ähnlicher Zugang wurde in der Krebstherapie bereits erfolgreich durch das Inhibieren von PARP gewählt, einem Protein, welches - ähnlich wie POLΘ – mit BRCA1 synthetisch letal ist. In der Praxis erwiesen sich die PARP-basierten Therapien zwar als sehr erfolgreich, allerdings zeigte sich auch, dass Patientinnen und Patienten im Rahmen der Therapie Resistenzen entwickelten. „Umso wichtiger ist es, die Prozesse unserer DNA-Reparaturmechanismen genau zu verstehen und zusätzliche, potenzielle Therapiepfade zu identifizieren“, so Loizou.
Quelle: idw/CeMM
Artikel teilen