Synthetische Moleküle in lebende Zellen geschleust
Durch diese Eigenschaften können die Wissenschaftler sogar die Selbstorganisation der „Designer-Moleküle“ in der Zelle verfolgen: „Mittels Fluoreszenzmikroskopie sehen wir, ob die Moleküle einzeln oder in Verbünden vorliegen. Zudem lässt sich beobachten, an welchem Ort und zu welcher Zeit die Selbstorganisation stattfindet“, erklärt Ziener weiter. Dabei sei alleine die Lokalisierung der Moleküle in der fluoreszierenden Zelle herausfordernd.
Hinweise auf Vorgänge im Zellinneren
Abhängig von der genauen Struktur bewegen sich die Moleküle über verschiedene Zellkompartimente bis in die Nähe des Zellkerns und bilden dort größere Molekülverbünde – oder sie reichern sich in den Mitochondrien, also den Zellkraftwerken, an. Dies lässt sich durch den Einsatz eines spezifischen pharmakologischen Inhibitors und die Erniedrigung der Temperatur kontrollieren: „Detailliertere Kenntnisse über diese Vorgänge im Zellinneren könnten auf längere Sicht zu einem gezielten Einsatz von Medikamenten führen, die beispielsweise an den Mitochondrien angreifen“, sagt Professor Holger Barth vom Institut für Pharmakologie und Toxikologie des Universitätsklinikums Ulm. Allerdings müsse noch weiter an der genauen Lokalisierung der Moleküle im Zellinneren geforscht werden. Schon jetzt gestatten die synthetischen Moleküle den Forschern jedoch ungeahnte Einblicke ins Zellinnere.
Zahlreiche Förderungen
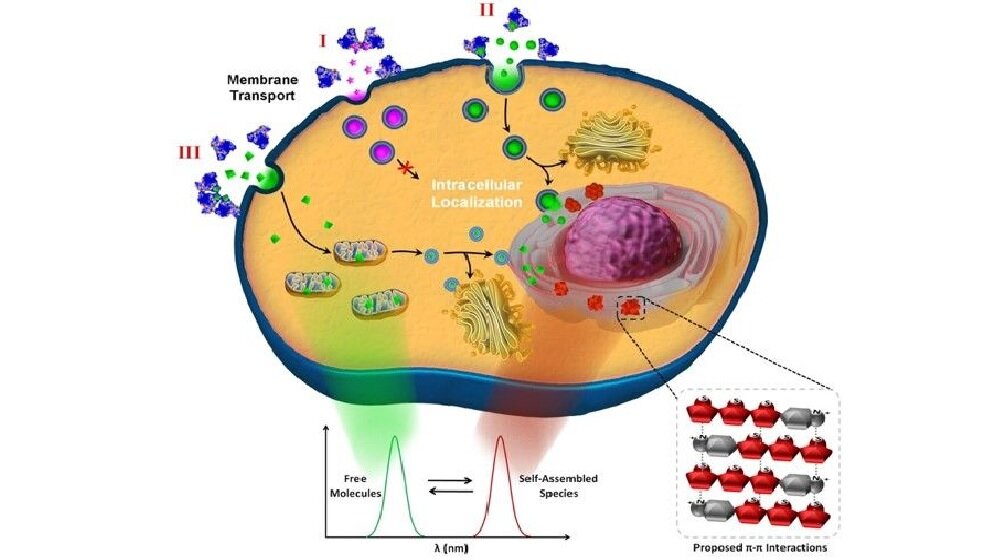
*Synthetische Oligomere werden mit Hilfe eines Komplexes mit humanem Albumin (HSA) in der Zelle aufgenommen. Über Fluoreszenz kann in Echtzeit zwischen dem molekular gelösten (grün) und dem aggregierten Zustand (rot) unterschieden werden. In Abhängigkeit von der Molekülstruktur werden verschiedene Zellkompartimente wie Endosomen, Mitochondrien oder zellkernnahe Strukturen angesteuert.
David Y.W. Ng, Roman Vill, Yuzhou Wu, Kaloian Koynov, Yu Tokura, Weina Liu, Susanne Sihler, Andreas Kreyes, Sandra Ritz, Holger Barth, Ulrich Ziener, Tanja Weil: Directing Intracellular Supramolecular Assembly with N-heteroaromatic Quaterthiophene Analogues. Nature Communications (2017). DOI: 10.1038/s41467-017-02020-2.
Artikel teilen