Können Blinde bald wieder sehen und Taube hören?
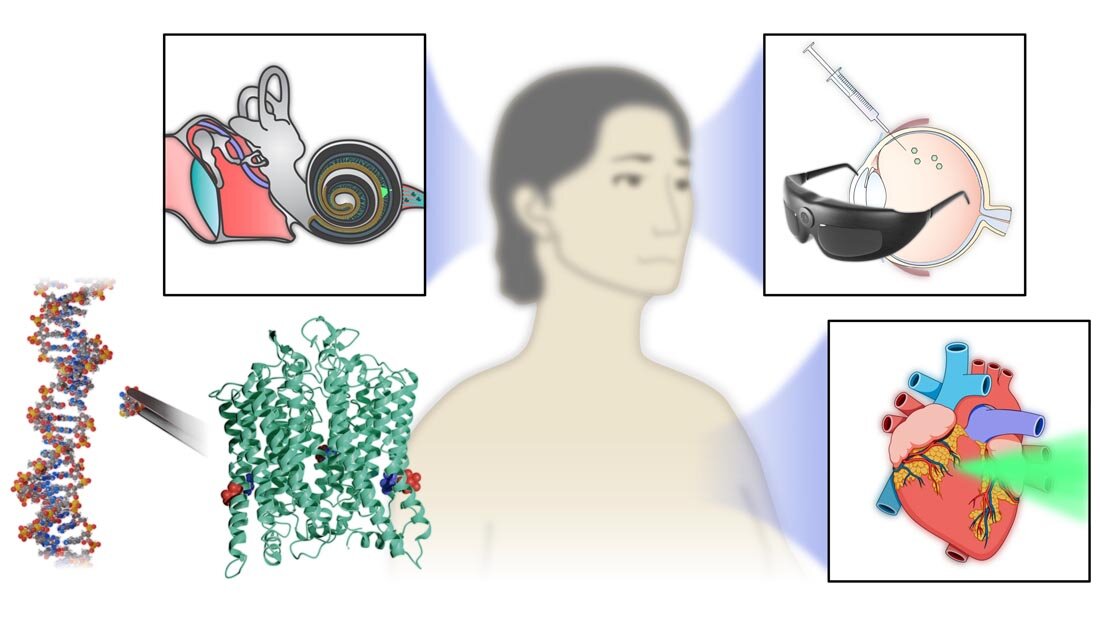
Es ist ein alter Menschheitstraum, Blinden wieder die Sehkraft und Tauben den Hörsinn zurückzugeben. Göttinger Forscherinnen und Forscher des Exzellenzclusters Multiscale Bioimaging (MBExC) und des Else Kröner Fresenius Zentrums für Optogenetische Therapien der Universitätsmedizin Göttingen (UMG) arbeiten an der Entwicklung innovativer Therapien zur Behandlung von Blindheit, Taubheit und Herzrhythmusstörungen. Die Optogenetik ist eine bahnbrechende Technologie, die lichtempfindliche Proteine, sogenannte Kanalrhodopsine, nutzt, um die Aktivität von Nerven- und Muskelzellen gezielt zu steuern. Die Baupläne für diese „molekularen Lichtschalter“ werden mittels spezieller Viren in die entsprechenden Zellen eingeschleust. Durch gezielt gesetzte Lichtpulse kann dann die Zellaktivität präzise an- und abgeschaltet werden. Das Feld der Optogenetik hat weltweit neue Möglichkeiten in der Grundlagenforschung, aber auch für die Behandlung von Erkrankungen eröffnet. Damit diese Technologie zur Entwicklung neuer Behandlungsmaßnahmen für beispielsweise herzkranke, schwersthörige und blinde Menschen genutzt werden kann, müssen sowohl die lichtempfindlichen Proteine als auch die Viren optimal angepasst werden, um den maximalen Nutzen und die erforderliche Sicherheit für die Anwendung beim Menschen zu gewährleisten.
Effizienz der optogenetischen Anregung deutlich gesteigert
Die Wissenschaftler haben jetzt die Entwicklung und Anwendung eines neuen, besonders vielversprechenden lichtempfindlichen Proteins beschrieben. Dieses vom Team um Dr. Thomas Mager, Arbeitsgruppenleiter am Institut für Auditorische Neurowissenschaften der Universitätsmedizin Göttingen (UMG), entwickelte neue Kanalrhodopsin trägt den Namen „ChReef“. „Durch die gezielte Veränderung des Bauplans dieses lichtaktivierbaren Proteins und den Einsatz von zum Teil roboterbasierten Analysemethoden, ist es uns gelungen, die Effizienz der optogenetischen Anregung deutlich zu steigern“, erklärt Dr. Mager. „Damit kommen wir einen ganzen Schritt weiter Richtung Anwendbarkeit beim Menschen, um den Seh- und Hörsinn wieder herzustellen und den Herzschlag zu regulieren“, so Prof. Dr. Tobias Moser, Direktor des Instituts für Auditorische Neurowissenschaften der UMG sowie MBExC- und EKFZ OT-Sprecher.
Herzmuskelzellen wieder richtig takten
In einer umfassenden Studie haben die Wissenschaftlerinnen und Wissenschaftler von MBExC und EKFZ OT die Effizienz des neuen Kanalrhodopsins geprüft und Belege für das große Potenzial von ChReef für die Biowissenschaften und die klinische Anwendung erbracht. Forscherinnen und Forscher um Prof. Dr. Dr. Tobias Brügmann, Arbeitsgruppenleiter am Institut für Herz- und Kreislaufphysiologie der UMG, MBExC-Mitglied und stellvertretender EKFZ OT-Sprecher, konnten beispielsweise zeigen, dass das neue „Werkzeug“ unregelmäßig schlagende Herzmuskelzellen mit sehr geringem Energieaufwand wieder in den richtigen Takt überführen kann.
Einsatz am Auge
In einer weiteren Studie, unter Leitung von MBExC-Mitglied und stellvertretende EKFZ OT-Sprecherin Prof. Dr. Emilie Macé, Professorin für „Dynamik erregbarer Zellnetzwerke“ in der Klinik für Augenheilkunde der UMG, wurde das neue Werkzeug blinden Mäusen in Form einer Gentherapie in die Augen eingeschleust. Ein anschließender Verhaltenstest zeigte, dass die Mäuse in der Lage waren, Helligkeitsunterschiede auf einem iPad-Bildschirm zu erkennen. Diese Art der Sehwiederherstellung wurde bereits im Rahmen anderer Studien am Menschen überprüft, allerdings waren mit den bisher verwendeten Kanalrhodopsinen sehr starke Lichtquellen notwendig.
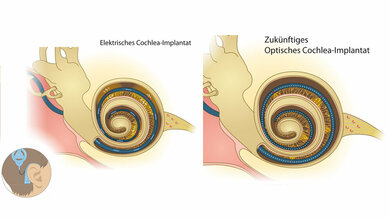
Einsatz bei optogenetischem Cochlea-Implantat
Eine weitere mögliche Anwendung von ChReef sehen die Forschenden in der optogenetischen Wiederherstellung des Hörens mittels optogenetischen Cochlea-Implantats (oCI). Dieses soll eine bessere Auflösung verschiedener Tonhöhen im Vergleich zum elektrischen Cochlea-Implantat versprechen, das derzeit weltweit zur Hörrehabilitation eingesetzt wird. In der nun veröffentlichten Studie benötigten die Forschenden für das „Hören mit Licht“ nur sehr geringe Lichtmengen. „Durch die Entwicklung von ChReef haben wir einen großen Schritt in Richtung klinische Anwendung des optogenetischen Cochlea-Implantats gemacht, da nun deutlich weniger Energie für das ‚Hören mit Licht‘ benötigt wird“, erläutert Prof. Moser. „Zum einen reduzieren sich dadurch die Schädigungen der Zellen durch Licht, zum anderen halten die Batterien länger.“ Für die Anwendung am Menschen ist ebenfalls relevant, dass die Wiederherstellung des Hörsinns mit Licht auch im Primatenmodell möglich ist, wie Wissenschaftlerinnen und Wissenschaftler um Prof. Dr. Marcus Jeschke, Leiter der Forschungsgruppe „Kognitives Hören bei Primaten“ am Deutschen Primatenzentrum – Leibniz-Institut für Primatenforschung (DPZ), in Göttingen zum ersten Mal zeigen konnten. „ChReef stellt einen bedeutenden Fortschritt in der Optogenetik dar und bietet großes Potenzial für die Grundlagenforschung aber auch für die therapeutische Anwendungen, etwa bei Herzrhythmusstörungen oder der Wiederherstellung von Hör- und Sehsinn“, ergänzt Dr. Bettina Wolf, Postdoktorandin am Institut für Auditorische Neurowissenschaften und Koautorin der Studie.
Quelle: idw/UMG
Artikel teilen