Ein Forschungsteam vom Center for Molecular Medicine Cologne (CMMC) der Universität zu Köln konnte zeigen, dass das Protein cFLIP entscheidend ist, um die Abwehrkräfte des diffus großzelligen B-Zell-Lymphoms (Diffuse Large B Cell Lymphoma – DLBCL) gegen den programmierten Zelltod zu überwinden. Diese Abwehrkräfte machen eine Behandlung oft unwirksam, weil sie es den Krebszellen ermöglichen, zu überleben. Die Ergebnisse seien besonders relevant für ABC-DLBCL, einen spezifischen Subtyp des Blutkrebses mit einer schlechten Prognose für Patientinnen und Patienten sowie einer niedrigen Überlebensrate.
Alternative Behandlungsmethoden benötigt
Das DLBCL ist die häufigste Form des Non-Hodgkin-Lymphoms, einer Krebsart, die sich aus bestimmten weißen Blutkörperchen, den Lymphozyten, entwickelt. Bei der derzeitigen Frontline-Immunchemotherapie wird der Antikörper Rituximab mit Chemotherapeutika kombiniert. Circa 60 Prozent der Betroffenen können damit zwar geheilt werden, doch etwa 50 Prozent der Behandelten erleiden einen Rückfall oder sprechen nicht auf die Behandlung an. Dies erschwert weitere Therapieversuche. Das Forschungsteam betont deshalb, dass es dringend erforderlich sei, alternative Behandlungsmethoden zu finden. Ein Weg könnte die Suche nach Schwachstellen in DLBCL-Zellen sein. Doch dies gestaltet sich schwierig, da DLBCL sehr heterogen ist. Außerdem entgehen DLBCL-Zellen dem programmierten Zelltod (Apoptose), indem sie verstärkt den Schutzfaktor BCL2 bilden. Dieser verschafft den Lymphomzellen einen Überlebensvorteil. Deshalb sei es entscheidend, die Mechanismen zu verstehen, die den Zelltod in Lymphomzellen steuern. In einem nächsten Schritt sei es wichtig, Wege zu finden, die durch die Überproduktion des Proteins BCL2 verursachte Blockade der Apoptose zu überwinden. Die Hoffnung: Dann ließe sich der Zelltod wieder aktivieren.
Besonders resistente DLBCL-Zellen
Es gibt verschiedene Arten des Zelltods: Das BCL2-Protein steuert eine davon, die sogenannte intrinsische Apoptose. Zellen können jedoch auch über einen anderen Weg – die extrinsische Apoptose – absterben, die durch das cFLIP-Protein streng kontrolliert wird. Das Forschungsteam unter der Leitung von Dr. Alessandro Annibaldi am CMMC hat nun entdeckt, dass DLBCL-Zellen neben BLC2 auch cFLIP überproduzieren. Auf diese Weise sind sie in der Lage, sowohl den intrinsischen als auch den extrinsischen Zelltod abzuwehren und dadurch sehr resistent zu werden. „DLBCL-Zellen bauen Straßensperren, um die intrinsischen und extrinsischen Zelltodwege zu unterbrechen mit dem Ziel, unsterblich zu werden und einen Überlebensvorteil gegenüber normalen Zellen zu erlangen. Wir wollten das Hindernis auf dem Weg der extrinsischen Apoptose identifizieren und es dann beseitigen, um das Schicksal dieser Zellen umzuprogrammieren und ihren Tod herbeizuführen. Bereits seit Langem bestand die Vermutung, dass ein solches Hindernis existiert. Nun konnten wir es erstmals nachweisen und seine klinische Bedeutung aufklären“, sagt Annibaldi.
ABC-DLBCL-Zellen abtöten?
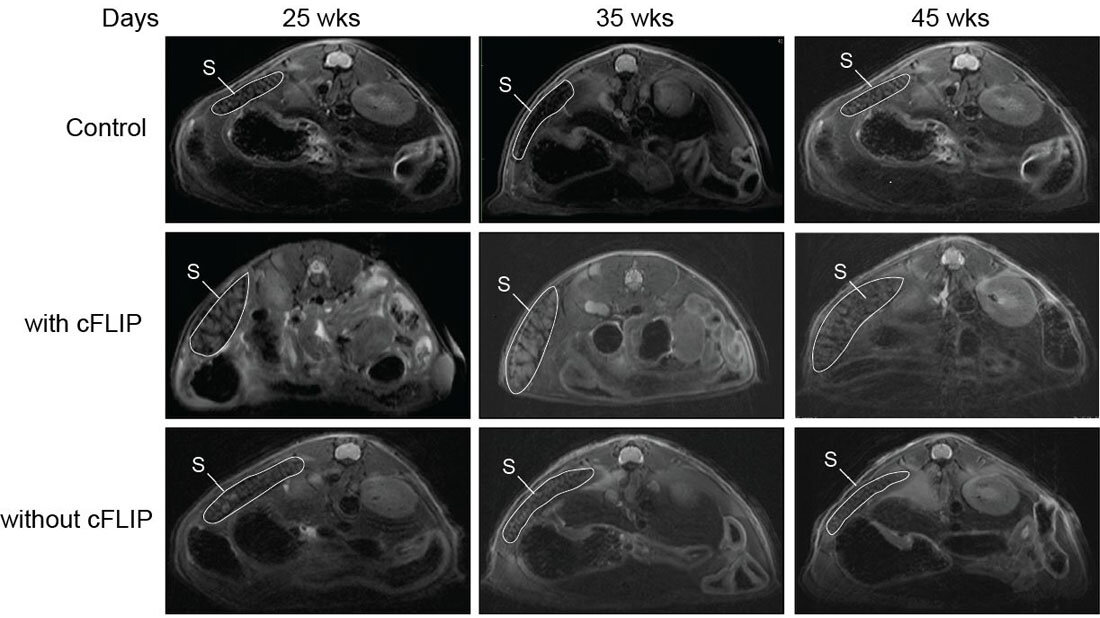
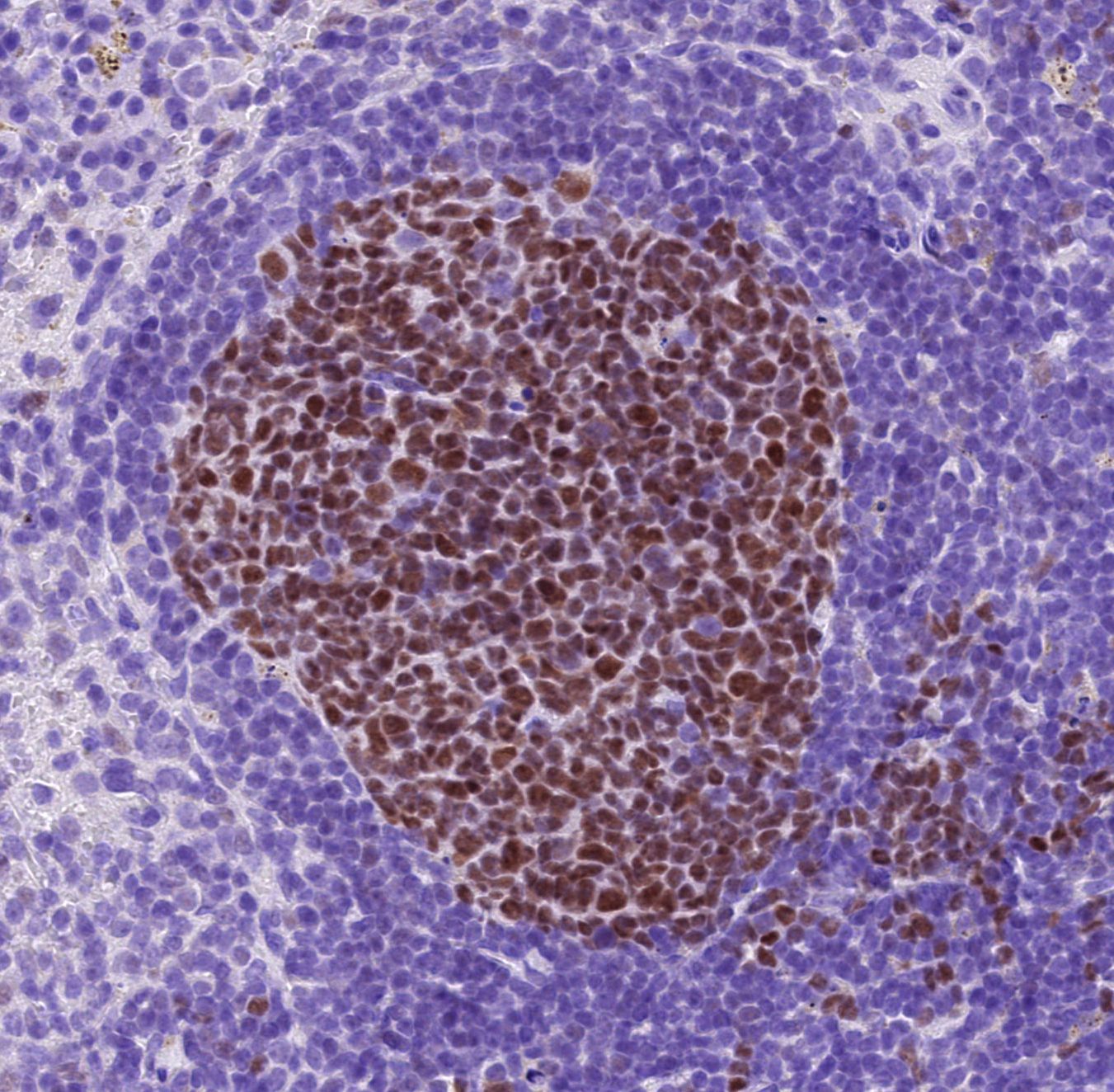
Die Wissenschaftler/-innen verwendeten für ihre Studie modernste zell- und molekularbiologische Techniken sowie ein präklinisches Mausmodell für DLBCL. So konnten sie herausfinden, dass ein gezielter Angriff auf cFLIP die durch BCL2-Überproduktion vermittelte Blockade der Apoptose aufheben und den Zelltod in Lymphomzellen wieder aktivieren kann. Es konnte gezeigt werden, dass cFLIP speziell im Subtyp ABC-DLBCL überexprimiert wird. Werde cFLIP eliminiert, können die Lymphomzellen für Todessignale re-sensibilisiert und die Entwicklung des Lymphoms verhindert werden, so das Team. Entsprechend könnte damit der Grundstein für die Entwicklung von Medikamenten, die gezielt auf cFLIP abzielen, gelegt werden. Solche Medikamente könnten, allein oder in Kombination mit anderen Medikamenten, ABC-DLBCL-Zellen abtöten – unabhängig davon, welche Mutationen sie tragen, solange sie cFLIP produzieren. „Der Einsatz von cFLIP in Kombination mit bestehenden Therapien stellt eine vielversprechende Option dar, die für Patientinnen/Patienten, die auf andere Standardbehandlungen von DLBCL nicht ansprechen, weiter untersucht werden sollte“, sagt Doktorandin Kristie Bariboloka, die die Forschungsarbeit im Labor leitete.
Quelle: Uni Köln
Artikel teilen