Mukoviszidose: Nanobody repariert CFTR-Kanal
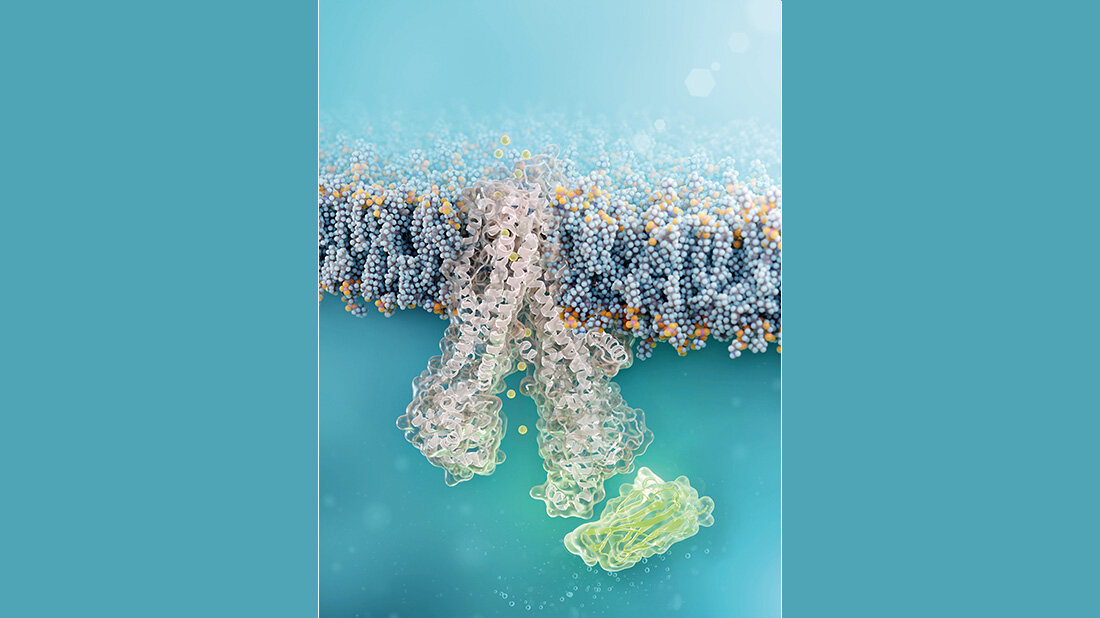
Fast 90 Prozent der Betroffenen der Mukoviszidose leiden an einer Mutation im CFTR-Kanal. Dieser Kanal reguliert den Wasser- und Salztransport in der Lungenschleimhaut, sodass dieser flüssig genug ist. Die als F580del betitelte Mutation sorgt dafür, dass an Position 508 eine Aminosäure fehlt, der CFTR-Kanal sich falsch faltet und damit nicht mehr aktiv in der Zellmembran arbeiten kann. Der Schleim ist dadurch zu zäh und auch Erreger können nicht mehr richtig abtransportiert werden. Die Lungenfunktion verringert sich dadurch und es kommt zu einer chronischen Infektion und Entzündung der Atemwege.
Nanobody repariert Gendeffekt
Ein Team der Charité arbeitet schon seit mehreren Jahren daran, die Behandlung der Mukoviszidose zu verbessern. Denn bisher besteht die Therapie aus einer Kombination von Elexacaftor, Tezacaftor und Ivacaftor, die zwar die Funktion des CFTR-Kanals auf etwa 50 Prozent anheben kann, doch die chronischen Entzündungen und Infektionen bleiben bestehen – wenn die Therapie denn anschlägt. Die Forschenden entwickelten daher einen Antikörper, der den CFTR-Kanal stabilisieren soll. Der Nanobody kann sich präzise an den Proteinen des Kanals anlagern. Chemisch ist er mit einem Transportsignal versehen, wodurch er in die Schleimhautzellen der Lungen eindringen kann. Der Nanobody bringt den CFTR-Kanal in Form und gibt ihm die Funkionsfähigkeit zurück.
Für 24 Stunden kann der Nanobody an den mutierten CFTR-Kanal binden. Funktionelle Untersuchungen zeigen, dass der Nanobody keinen Schaden anrichtet und der CFTR-Kanal wieder Chlorid transportieren kann. Gemeinsam mit der Dreifachtherapie zeigt sich ein Synergieeffekt: zusammen schaffen sie es, die Funktion des CFTR-Kanals auf 90 Prozent des Normalniveaus anzuheben.
Vollständig neuer Wirkmechanismus
„Es handelt sich, neben dem präklinischen Machbarkeitsnachweis einer Reparatur des CFTR-Kanals, um das erste Beispiel eines funktionalen zellpermeablen Antikörpers: Bisher wurden zellgängige Nanobodys vor allem zum Sichtbarmachen intrazellulärer Zielstrukturen oder zur gezielten Abtötung von Zellen eingesetzt“, erläutert Prof. Dr. Christian Hackenberger, Chemiker vom Leibniz-FMP, dessen Team den Nanobody entwickelt hat. Der neue Wirkmechanismus ermöglicht es, die CFTR-Funktion fast vollständig zu normalisieren. Damit lässt sich die Behandlung der Mukoviszidose weiter verbessern und legt einen neuen Grundstein für einen breiteren therapeutischen Einsatz.
Bis zur klinischen Anwendung müssen jedoch noch die genauen Wirkweisen geklärt werden und wie das Immunsystem auf eine Nanobody-Behandlung reagiert. Doch auch bei anderen genetischen Erkrankungen könnte die intrazelluläre Nanobody-Therapie zur Anwendung kommen.
Quelle: idw
Artikel teilen